
(SkyPat © Pathology from 1996)
Stort senter og samling angående patologi og fakta Vev Celler Mikroskop Immunologi Genetikk
Pathologie - Norwegen, La Norvège Kreft Senter - Cancer center - Zentrum blog Diagnostic and Prognosis Scientific Medicine - Vitenskapelig Medisin -
Evidencebased Pathology 2022 SkyPat © Tønsberg Vestfold Oslo
FLERE linker som bør besøkes, og hvor flere er mere moderne via Wordpressplattformen:
Wordpress: Patologi med Wordpress.
Wordpress: Skypat med Wordpress. Rikt om Klima og vær.
Wordpress: SCIENCE TVILER Blogg Norway.
Nye direkte lenker med Wordpress:
klimafakta.com Rikt om Klima og vær.
CORONAVIRUS - SARS er ikke nytt!
Studies of Severe Acute Respiratory Syndrome Coronavirus Pathology in Human Cases and Animal Models.Severe acute respiratory syndrome (SARS) outbreak of 2003
Aggregation and Prion-Like Properties of Misfolded Tumor Suppressors:
PATHOLOGY OUTLINES.com, find pathology information fast
PATOLOGI OG SKYPAT- for helse, naturvitenskap, realisme og fornuft.
Digital patologi ger kortare väntetider i cancervården. Linköpings Universitetssjukhus, Sverige.
COCHRANE Library. Trusted evidence. Informed decisions. Better health.
? PTLD/ Posttransplant lymphoproliferative disease, noe liknende som funn ved
Diffusion Chamber Cultur fra 1970-80 årenee?
NEWS: Google's Deep Learning AI project diagnoses cancer faster than pathologists
NEWS: Detecting Cancer Metastases on Gigapixel Pathology Images
Nice LINK: High Quality Pathology Image. Visual Survey of Surgical Pathology
CancerIndex. The Guide to Internet Resources for Cancer family of Web sites, established 1996
Malignes melanom. Universitats Klinicum, Freiburg. 2015.
Pioneers and leaders in microscopy by Dr Rebecca Pool

Patologene er ekspert på diagnoser, stiller kreftdiagnosene og mange andre pasientdiagnoser!
Kunnskap for din riktige diagnose, behandling og prognose!
Faglig kompetanse- din sikkerhet som pasient!
Patologi med focus på deg og pasientene!
Patologi før behandling!
Without pathology, there is no medicine!
BIRGER FREDRIK MOTZFELDT LAANE . M.D.
Physician and Consultant Pathologist
The very first Pathology Web page in Scandinavia (19.May 1996) !
![]() No .
since
9.15.1996:
No .
since
9.15.1996:

On the second Wednesday in November, International Pathology Day offers a platform for pathology and laboratory medicine services to address global health challenges.
Over 150 år med akademisk patologi i Norge!
Emanuel Fredrik Hagbert Winge.1ste professor i patologi
20. sept. 1866
The Norwegian Society of Pathology. 100 års Jubileum i 2023 !
Anbefaler boken: The Finel Diagnosis, Arthur Hailey A young pathologist and his efforts to restore the standards of a hospital controlled by an ageing, once brilliant doctor. One foulty diagnosis, one irrevocable error, precipitates tragedy.
Les også: Anonyme leger, William Mc. Kee German. Oversatt av Terje Strand, Oslo 1946.
Menu:? Patologi ?
Salivary gland/ Gl. thyreoidea
STEM CELLS/ Metastatic cancer/ unknown primary site Consensus/Dispute/Error in Pathology. Quality. Parasite, more, go to zoonosis -------------------------------------
Microscopic::Brunsnegle Slug Iberiasnegl areon vulgaris lusitanian slug spanish slug Lyme disease Ixodes ricinus Borrelia |
---------------------------------------------------------
|
Det er patologene som stiller bl. a. kreftdiagnosene
.
Som JANUShodet fra Vatikanet.
Patologi :
”Ser bakover og fremover i daglig arbeid”
Vi undersøker f.eks. om det hos pasienten foreligger forstadier til kreft, manifest kreft, type kreft, om den er hurtigvoksende og har spredt seg. Mange av pasientprøvene dreier seg om denne problematikk og antallet stiger pr. år. Diagnosesvarene blir ofte kommentert med forklaringer og råd til den rekvirerende lege. Diagnosen sier noe om sykdomsprognosen og behandlende lege kan så på riktig måte videre undersøke eller behandle pasienten. Patologene dekker et nødvendig behov for behandlende leger og samarbeide med andre leger er derfor viktig.
Patologen stiller også diagnosene fra annet mottatt pasientmateriale, med forandringer og abnormiteter i syke celler, vev og organer.
PATOLOGI : PASIENTBEHANDLING VIA MIKROSKOPET!
Selv om mikroskopering er en gammel teknikk, er tolkningen av mikroskopbildene ofte gullstandard for sykdomsprosessen.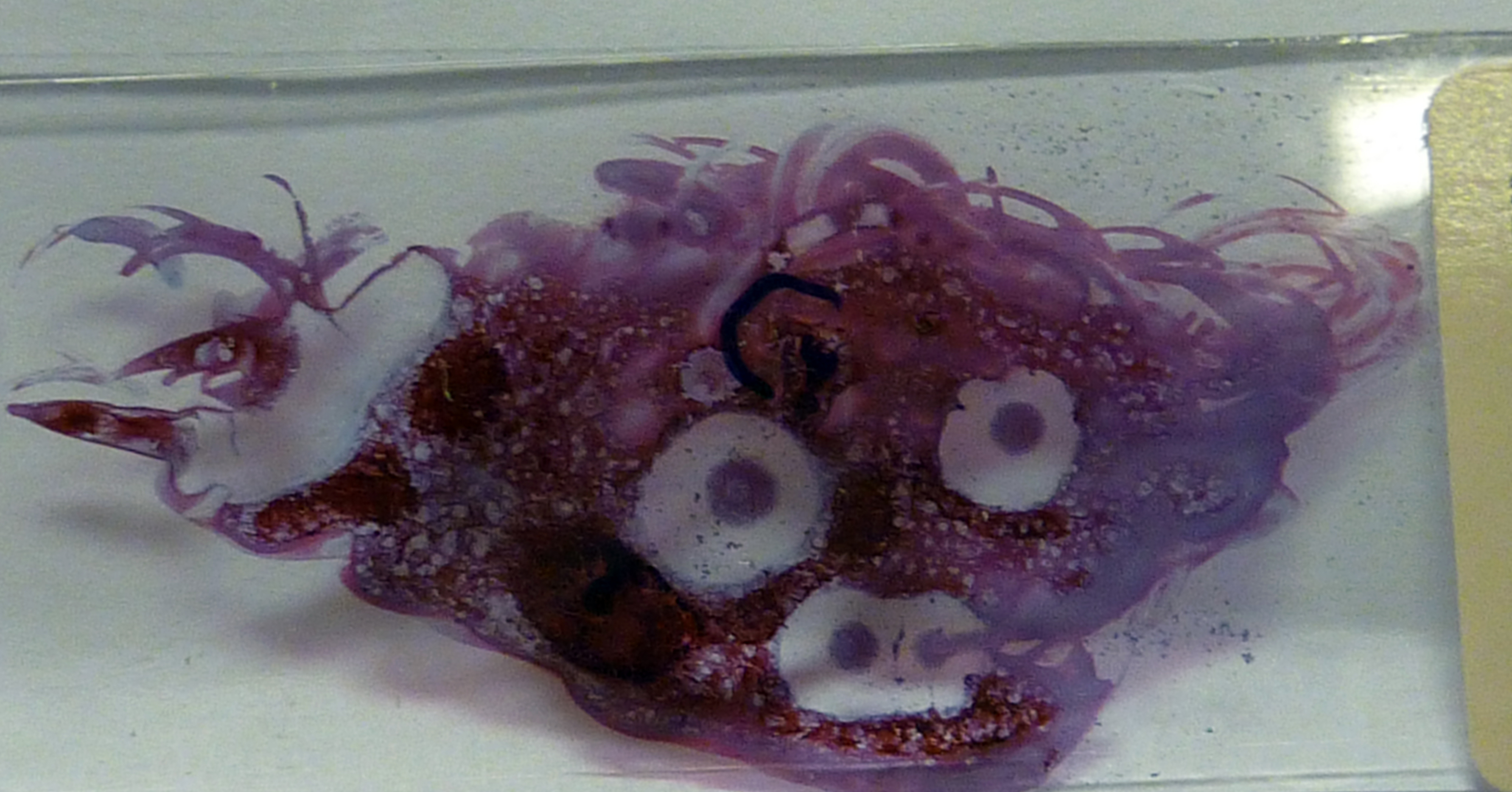 Det foreligger enorm informasjon i de mikroskopiske bildene. Som kjent kan man si at hva du ser i verden med dine øyne og også ved hjelp av mikroskop gjelder:
Det foreligger enorm informasjon i de mikroskopiske bildene. Som kjent kan man si at hva du ser i verden med dine øyne og også ved hjelp av mikroskop gjelder:
DET VANSKELIGSTE AV ALT ER Å SE DET SOM LIGGER RETT FORAN ØYNENE DINE!
Was ist das Schwerste von allem? Was dir das Leichteste dünket. Mit den Augen zu sehn, was vor den Augen dir lieget. Quelle: Xenien aus dem Nachlaß 45 (Johann Wolfgang von Goethe).
Det har kommet mange andre sofistikerte medisinske apparater og undersøkelsesmetoder i helsevesenet for å stille pasientdiagnoser for behandling, men en del gir ikke resulteter eller tolkningsforhold som er forenlig med den virkelige gullstandard- selv om helsepersonell mener dette. Man kan delvis si:
"A fool with a tool is still a fool"  Dessverre hører ofte en person bare på hva han tror han forstår (Goethe).
Dessverre hører ofte en person bare på hva han tror han forstår (Goethe).
”Thus I learned early on the great importance of a
close correlation between clinical and pathological
studies.
Each complements and supplements the other; it is
impossible to do intelligent surgery without a
thorough understanding of the pathology of disease
and it is equally impossible to make an intelligent
interpretation of pathology without a clear understanding
of its clinical implications.”
Arthur Purdy Stout.
(Bok: ”Guiding The Surgeon `s Hand”, 1997, Editor
Juan Rosai)
Patologi som betyr sykdomslære, er et grunnleggende fag for helsepersonell og er med på å gi "skolemedisinen" vitenskapelig forankring. Faget omhandler sykdommenes årsak, mekanismer, sykdomsutvikling og hvordan de strukturelle og funksjonelle forandringene i organer, vev og celler blir ved de forskjellige sykdommer.
Denne kunnskapen har ført til at lege med patologiutdannelse er spesialist på å tolke forandringer og abnormiteter i syke celler, vev og organer. Arbeidsområdet dreier seg i våre dager altså mest om patologisk anatomi. Forandringene kan være synlig med det blotte øye, men mikroskopisk undersøkelse er helt nødvendig. Patologene prøver å finne ut hva som feiler pasientene og stille de eksakte diagnosene ved sykdommer.
F.eks. får kliniker (lege) og/ eller røntgenlege mistanke om at pasienten har kreft eller legen ønsker å utelukke dette. Lege tar vevs- eller cellemateriale fra pasienten og patologen vurderer og stiller deretter den eksakte diagnose. Dette gjelder også i forbindelse med mammografi for brystkreft og screeningundersøkelse for tykktarmkreft.
#
Den vanlige metastaselære; her noe fra
Store norske leksikon Olbjørn Klepp
Metastase, dattersvulst fra en kreftsvulst. Løsrevne kreftceller kan dele seg og gi opphav til nye kolonier av kreftceller utenfor den opprinnelige svulsten.
Når en kreftcelle og dens etterkommere har delt seg så mange ganger at cellehopen er blitt 1–2 mm i diameter, må kreftcellene «slå på» kjemiske signalsystemer (angiogenesemekanismer) som medfører at små blodårer og lymfeårer vokser inn i svulsten. Dette er nødvendig hvis svulsten skal oppnå tilstrekkelig ernæring av kreftcellene for videre vekst. En del av kreftcellene kan vokse gjennom disse åreveggene og følge væskestrømmen videre til det drenerende lymfesystemet, hvor det er innlagt lymfeknuter med store ansamlinger av immunceller som skal forsvare organismen både mot mikrober og om mulig nedkjempe kreftceller. Andre kreftceller følger blodstrømmen direkte til de neste fine silsystemene av kapillarer i andre organer, f.eks. til lungevevet.
Blant mange milliarder slike løsrevne kreftceller kan enkelte likevel lykkes i å slå seg ned blant normale celler i andre organer, ofte først i de regionale lymfeknutene. Slike spredte kreftceller kan dele seg ukontrollert i det nye organet og gi opphav til lokale metastaser. Disse vil igjen indusere innvekst av blodkar i metastasene, som kan vokse til store svulstmasser som så igjen sender ut nye kreftceller.
Det er en aktiv interaksjon mellom normalvevsceller, immunceller og kreftceller, hvor kreftcellene i visse tilfeller utnytter normale vekstfaktorer og endog immunangrep til lokal etablering og vekst.
Det er viktig å være klar over at metastasene vanligvis beholder mange av de biologiske egenskapene til primærsvulsten.
------------------------"---------------------------
Det er antatt at tendensen til spredning er liten når en kreftsvulst er liten. Dette peker på betydningen av tidlig diagnose og behandling. (Min bemerkning ??)
------------------------"---------------------------
Delvis tidligere "sannheter".
1. Lokal cancer er ofte utenom de lokale negative forhold, relativt ufarlig.
2. Når det oppstår metastaser blir canceren imidlertid meget alvorlig.
3. Vanligvis tenker man seg at metastaser vokser ut fra cancerceller som har reist fra tumor via lymfe/ blodbane.
3. Canceren består av bl. a. "ukontrollert" celleproliferasjon.
4. Selv om det ved vekst er en økning av cancerceller i tumor, er der også tilstede celledød /apoptose.
5. Canceren vokser i størrelse når celledøden av cancerceller er mindre enn celleveksten.
6. Cancerceller består av trolig bl. a. stamceller og tumorceller som har trolig "mindre betydning".
7. Den siste nevne celletypen dør lettere ved hjelp av medisinsk tumorbehandling, og tumor blir deretter ofte mindre etter slik behandling.
8. Stamcellene derimot lever trolig mer eller mindre videre etter kreftbehandling og de/ etterkommere kan trolig klinisk dukke opp etter mange år (mer enn30 år ?).
9. Canceren kan trolig være ytterst liten (2-3 mm.?) og kan alt ha alt gitt metastaser.
10. Mulig kommer det metastaser lettere etter manipulering av tumor, eller operativ fjerning av tumor (noe usikkert!).
11. Cancer kan også metastasere i annet arr-område.
12. Metastaser vokser ofte i områder med gode vekstbetingelser.
A. Tunneling nanotuber (TNT) er en nyppdaget form for celle-til-celle kommunikasjon.
B. Det foreligger en dynamisk lang-distanse forbindelse mellom animale celler.
Long-distance electrical coupling via tunneling nanotubes.
Xiang Wang, Hans-Hermann Gerdes
Cell-cell communication and growth control of normal and cancer cells: Evidence and hypothesis
Marc Mesnil, Hiroshi Yamasaki, Allan Balmain, J. Carl Barrett, Harold Moses
C. Det foreligger ett nanotubulært cellenettverk.
Vanligvis tenker man på at metastasene oppstår p.g.a. tumorceller vandrer og slår seg ned ett sted i kroppen!
Det foreligger teorier eller bevis om at også relativt nyoppståtte og ytterst små kreftsvulster kan alt ha metastasert til andre steder i kroppen. Mange tenker imidlertid på at tumorceller eller grupper av tumorceller fra en relativt stor og eldre kreftsvulst kommer inn i en sirkulerende veskebane og setter seg deretter fast i et område.
Det har imidlertid nå fremkommet forskning på at det hos kreftpasienter også forekommer fritt sirkulerende DNA, d.v.s. cellefritt DNA eller cfDNA fra cancersvulster som dør, blir ødelagt eller fra cancerceller som går i stykker i veskebanen.
Teoretisk kan vel således cfDNA materiale på et meget tidlig tidspunkt komme inn i normale celler i kroppen og sammen med DNAmaterialet til friske celler omdanne DNAmaterialet til materiale med kreftegenskap eller ligge mere eller mindre skjult i cellen en tidsperiode til andre omstendigheter som f.eks. nedsatt immunforsvar oppstår.
Arvelig sammenheng av kreftsvulster kan mulig også således forklares.
Visse kreftsvulster har en tendens til å metastasere til spesielle kroppsorganer eller kroppsområder. Dette kan mulig komme av tumortypen finner best vekstbetingelse i slike områder, noe liknende forhold som ved f.eks. planter.
Kreft er en sykdom hvor et økende antall unormale celler vokser i organismen. Disse kreftcellene er unormale både av utseende og oppførsel. De har tapt en del av de normale cellers egenskaper, og de har fått nye, unormale egenskaper. Kreftceller har tapt evnen til å reagere normalt på de vanlige reguleringsmekanismer for celledeling og/eller cellemodning. Derfor vokser det opp en svulst, og kreftcellene kalles for ondartede eller maligne celler. Vi regner at det er om lag 1 milliard celler per gram vev, dette gjelder både for normalvev og i kreftsvulster.
Når det gjelder utseende, er det større variasjon i størrelse og form blant kreftceller enn blant normale celler. Særlig kjernen er unormal hos kreftceller, og inneholder ofte mer kjernesubstans enn vanlig. Kreftcellene har som regel også tapt evnen til normal funksjon.
Kreftcellene har fått den egenskap at de kan vokse inn i tilstøtende vev og organer, og dette kaller vi infiltrerende vekst.
Utvikling fra normalcelle til kreftcelle skjer vanligvis trinnvis. Fellesnevner er endringer (mutasjoner) i gener i arvestoffet (DNA), som styrer sentrale reguleringsmekanismer for cellevekst og celledeling. Dette kan medføre øket stimulering av celleveksten ved økning av kjemiske signaler og/eller reseptorer (mottakerapparat for signalene), bortfall av bremsmekanismer, eller at kreftcellene ikke begår programmert selvmord (apoptose). Ved skade av gener som styrer kontroll- og reparasjonsmekanismer for DNA, øker frekvensen av ureparerte mutasjoner, noe som aksellererer kreftutviklingen. Det må oftest til minst 5 – 10 endringer av sentrale reguleringsmekanismer i cellen og dens datterceller, før man har en fullt utviklet kreftsvulst.
Karsinom in situ, betegnelse på celleforandringer som tyder på begynnende kreftutvikling uten at spredning ennå har begynt. Begrepet er særlig brukt om forstadier til kreft i livmorhalsen, hvor en enkel celleprøve (cytologisk prøve) kan avsløre slike forandringer, og pasienten kan bli behandlet og helbredet ved et enkelt kirurgisk inngrep. Karsinom in situ forekommer også bl.a. i brystkjertler og i testikkelvev.
En kreftsvulst, dvs. en ondartet svulst, vil derimot ofte ikke respektere naturlige grenser. Den vil tvert imot vokse utover disse og inn i nabovev og naboorganer, dvs. infiltrere i det omgivende normalvevet.
Normalt holder celler og vev hverandre i likevekt i kroppen ved hjelp av kompliserte reguleringsmekanismer som kun delvis er kjent. Dersom det er økt behov for celler, vil celledeling i de fleste vev øke til behovet er dekket, for så å avta igjen. I svulster er denne likevekten forstyrret, og cellene vokser autonomt, dvs. selvstendig, uten å bli stoppet av reguleringsmekanismene.
----er en svulst en neoplasi som kan påvises som en distinkt kul, knute eller fortykkelse.
Den sykelige forandringen er i arvestoffet (DNA) i kjernen til kreftcellene og involverer på ulik måte vekstkontrollgenene.
---------------------------------------
Vanlige aksepterte teorier innen patologi, men ikke passende funnforhold:
Cancer oppstår i en celle som deler seg videre og disse igjen videre og videre. (Trinnvis celledeling/ vekst). Eksponentiell vekst eller eksponentiell økning. (Når en størrelse øker med en fast prosent over like store tidsrom).
Usikkert? Man har vel nærmest aldri sett en eller noen få enkeltliggende cancerceller i vev.
Med slik vekst ville vel tumor stort sett trolig være mer eller mindre rund, noe som stort sett ikke er vanlig.
Tumor er dog oftest multifokal, også med satellitter.
---------------------------------------
Tidligste forandring/ vekst er ukjent.
Hvorfor en celle går over fra å være normalceller til atypisk/ cancercelle er mer eller mindre ukjent.
(Slumrende gener slås på/ mulig en del andre mer eller mindre kjente primære eller sekundære årsaker/ årsakssammenheng).
Mulig får stamtumorcellene også næring tilbake via nanotubenettverket, fra lengere vekkliggende celler, også mulig fra "normale/ friske" celler, for lettere å overleve/ vokse!
#########################################
The Biopsy Process & Report in English, writer Ed Uthman, M.D.
 Fremstillingsprosess
Fremstillingsprosess
Arbeidsredskapet er vesentlig mikroskopet hvor vi undersøker og vurderer små vevsprøver eller større operasjonspreparater /biopsi og celleprøver /cytologi, tatt både fra friske screening / masseundersøkelse og fra syke mennesker.
Vevsmateriale som klinisk lege har tatt fra pasient får vi oftest på fikseringvæske (formalin) . Små vevsprøver eller store organer undersøkes og riktige og tilstrekkelig antall vevsbiter skjæres ut og legges i kapsler. Biopsimaterialet skal gjennom en rekke forskjellige væsker før til det blir innstøpt i parafin. Da er vevsmaterialet så hårdt at det kan skjæres i meget tynne snitt. Disse snittene viderebehandles slik at vev til slutt får forskjellige farvenyanser. Det finnes mange spesialfarver som hjelper patologen i det diagnostiske arbeidet. Bioingeniører er her viktige medarbeidere.
Cellemateriale tatt fra pasient blir som oftest mottatt som utstryk på objektglass men også som kroppsvæske. Materialet blir viderebehandlet for til slutt å få fremstilt farvede celler på objektglass. Mikroskopisk forhåndsundersøkelse i cytologi (f. eks. masseundersøkelse/ screening mot livmorhalskreft) utføres av spesialtrente bioingeniører før patolog vurderer materialet og fastsetter diagnosen. Mye av arbeidet og funn dokumenteres og beskrives skriftlig.
Cervixscreening, bilde forstadium til kreft: 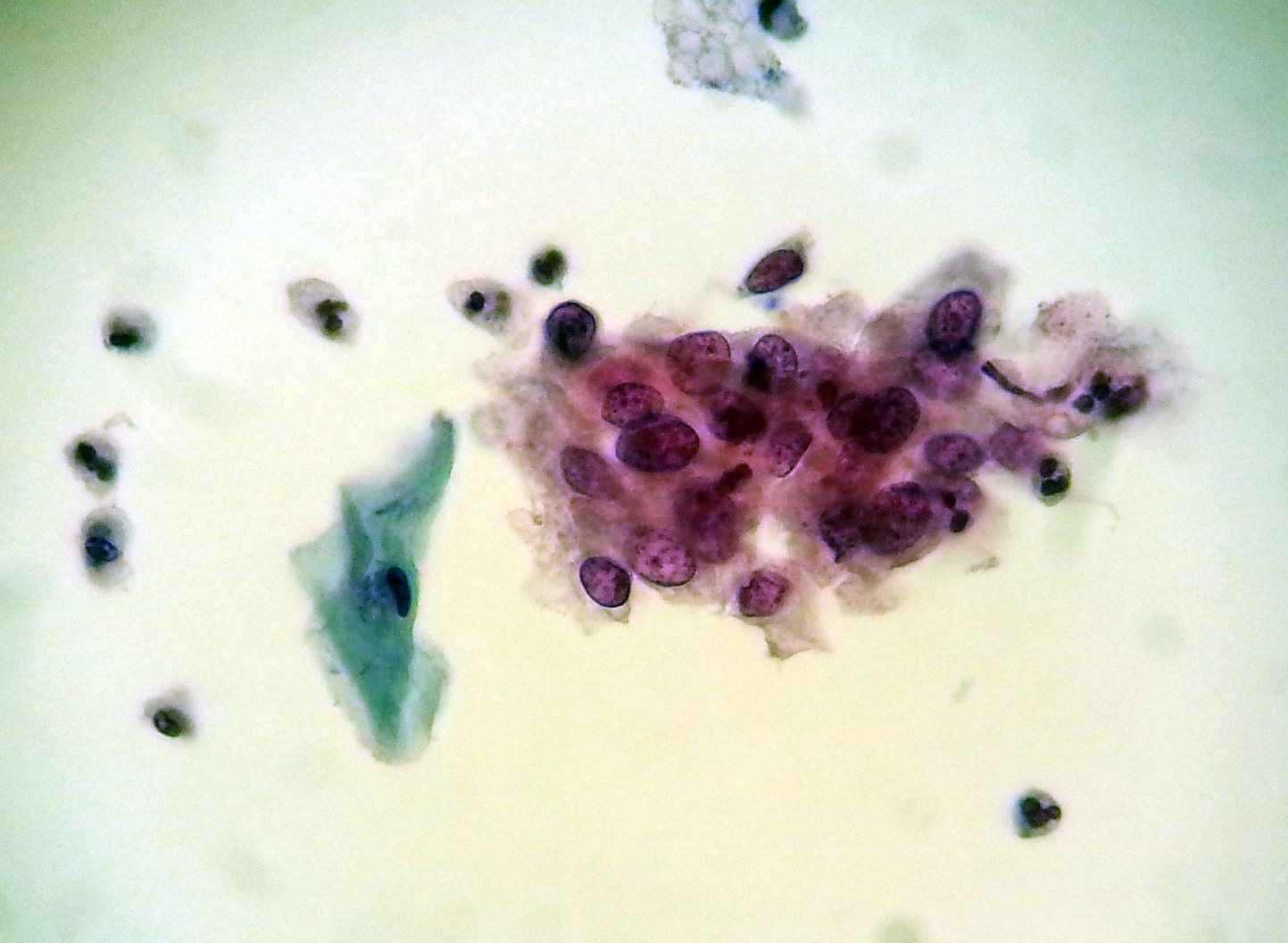
Diagnostisering 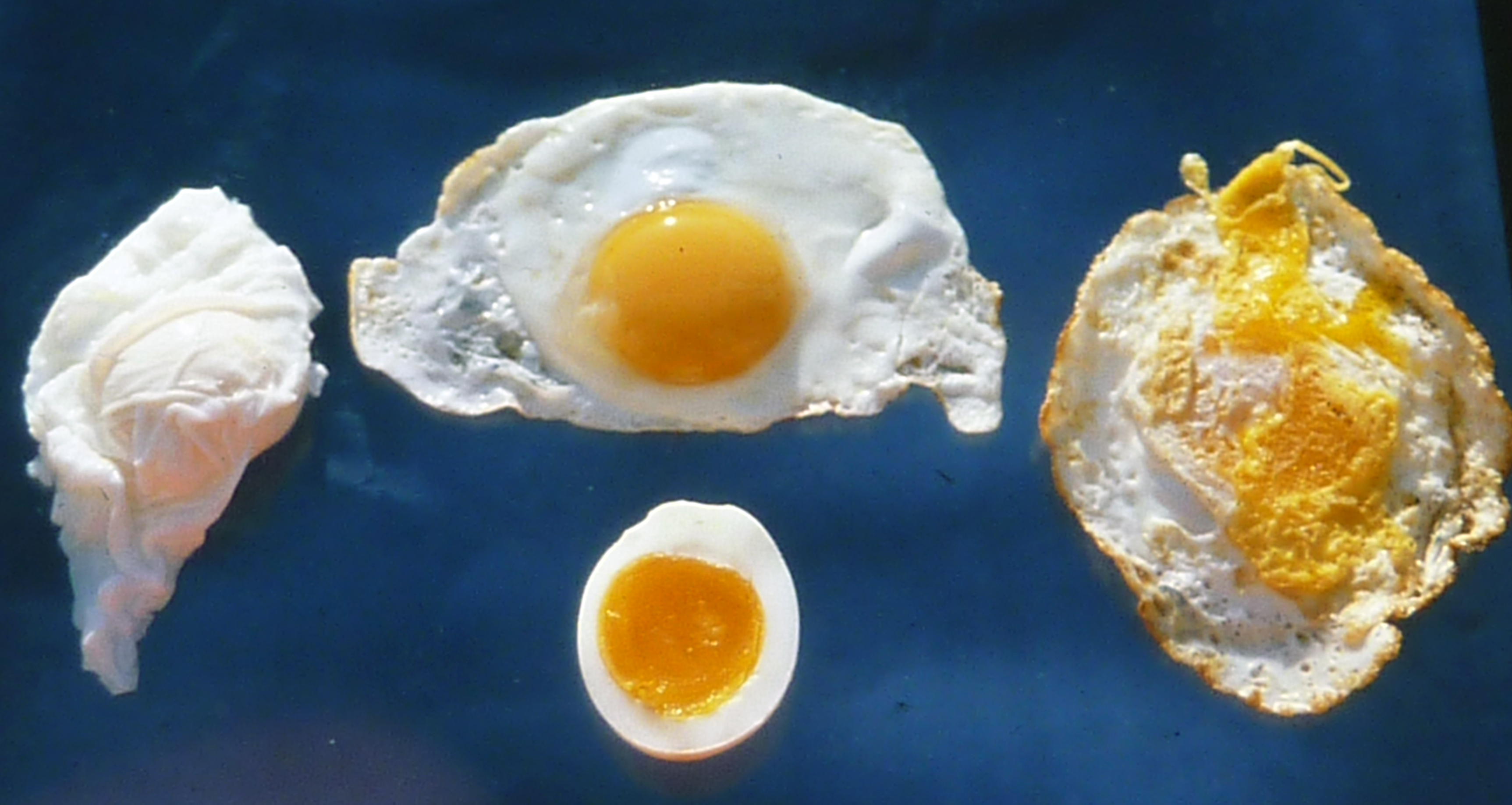
For å vurdere og diagnostisere er patologene mer eller mindre avhengig av at pasientenes lege bl. annet opplyser om hvor pasientmaterialet er tatt fra, og hvordan pasientmaterialet er behandlet. Her: Samme celle/ egg, men forskjellig behandling!
Arbeidet ved en avd. for patologi skiller seg vesentlig fra en laboratorieavdeling. Arbeidet er basert på personell og muligheten for automatisering eller maskinell diagnostikk er nærmest ikke tilstede. Faget ligner mere røntgenfaget hvor spesialutdannede leger også vurderer bildeforandringer.
På samme måte som ingen mennesker er like er heller
intet celle- eller vevsbilde helt likt ett annet. Det fins mange krefttyper,
differensieringer og stadier i forskjellige organer og ofte er det glidende
overganger. Kompleksiteten gjelder også de andre sykdomsgruppene.
Ofte mottar vi bare sparsomt materiale fra sykdomsområdet. Slike forhold
gjør at vurderingen og diagnostiseringen er innviklet eller vanskelig.
Det er nødvendig med adekvate kliniske opplysninger om pasienten og
materialet, tilgjengelig og stor litteraturmengde og at vi stadig oppdaterer
våre kunnskaper. Vevs- og cellemateriale ved avdelingen må være
stort og varierende. Eventuelt tidligere materiale fra pasienten skal være
tilgjengelig (alle snitt med celle- og vevsbiter/ snitt arkiveres for fremtiden).
Imidlertid kan ingen patolog beherske hele patologien. Mye av diagnostiseringen
bygger på erfaring og nå og da er det viktig at flere patologer
kan vurdere de samme forandringene. Det hender at snitt og materiale blir
sendt til andre patologer i Norge til spesialvurdering og også til patologer
i utlandet som man mener har mest erfaring i det spesielle tilfellet.
Vurderingen kan være så vanskelige at patologer stiller noe forskjellige
diagnoser og at man ikke kan avgjøre hvem som har rett eller om noen
i virkeligheten har rett. I slike tilfeller er det bare tiden som viser resultatet.
Dette må man dessverre leve med, for det fines ingen annen eller bedre
diagnostisering. I praksis blir det i slike tilfeller hvor man ennå
ikke helt har fastslått diagnosen allikevel utført en adekvat
pasientkontroll og behandling.
For lettere å diskutere faglige spørsmål har en del patologiavdelinger begynt med telepatologi hvor avdelingene og mikroskop er sammenknyttet med bilde og lyd. Dette er en undergruppe av telemedisin som er i rivende utvikling og som man bør satse på.
Det har i de senere år kommet mange nye undersøkelsesmetoder
som kan gi patologene mere informasjon til vurderingen og således komme
nærmere målet, f.eks. immunhistokjemi 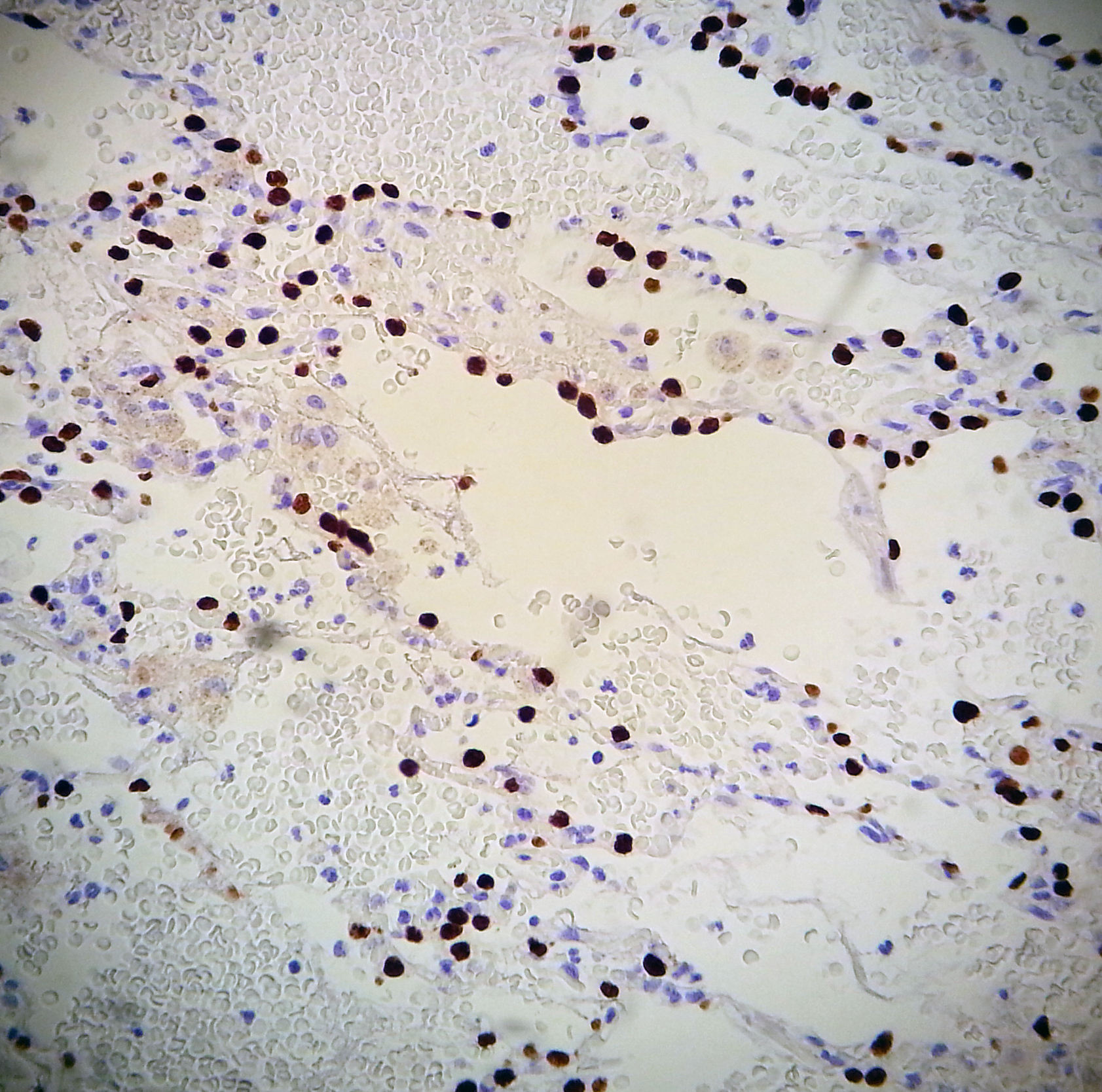 , genteknologi, molekylærpatologi
og avanserte telle- og målemetoder /flowcytometri. Alt har imidlertid
sin begrensning og det finnes f. eks. ingen tekniske metoder til sikkert å
skille ufarlige celler eller vev fra kreft eller forstadier til kreft. Slike
vurderinger baserer seg på godt, solid faglig skjønn.
, genteknologi, molekylærpatologi
og avanserte telle- og målemetoder /flowcytometri. Alt har imidlertid
sin begrensning og det finnes f. eks. ingen tekniske metoder til sikkert å
skille ufarlige celler eller vev fra kreft eller forstadier til kreft. Slike
vurderinger baserer seg på godt, solid faglig skjønn.
Frysesnitt
Ved vanlig diagnostisering tar det flere dager før patologen har kommet frem til diagnosen og vurderingen. Imidlertid med såkalt "frysesnitt" kan vev fjernet under pågående operasjon bli frosset ned slik at vevet kan skjæres i tynne snitt og farves. Dette blir mye brukt ved kreftproblematikk, f. eks. ved spørsmål om brystkreft. Etter vurdering av patolog blir svaret tilbakemeldt til legen som opererer. Vedkommende får således informasjon til hva man videre skal gjøre, f. eks. fjerne brystet. Denne raske informasjon og at pasienten slipper flere operasjoner gjør at metoden er utmerket, men vurderingen for patologen er vanskeligere enn ved vanlig prosedyre p.g.a. at de mikroskopiske snitt blir teknisk dårligere.
Punksjonscytologiske undersøkelser (kortversjon)
Det finnes en undersøkelsesform som er meget rask, skånsom for pasienten, billig og god å bruke innen kreftdiagnostikk, nemlig punksjonscytologi. Lege stikker en sprøytenål inn i det vevet hvor man ønsker å få materiale til diagnostisering, f. eks. i en svulst. Nålen kan også veiledes ved hjelp av røntgen eller ultralyd. Deretter trekkes cellemateriale ut til videre behandling og mikroskopisk undersøkelse. Flere og flere steder på kroppen er blitt tilgjengelig for dette opplegg. Metoden blir mye brukt i forbindelse med spørsmål om kreft og har stor betydning ved brystkreftscreening.
Det har vist seg at det beste resultatet for å få godt vurderbart materiale er at patologen selv tar prøven fra pasienten (punksjonsstasjon). Dette skjer også på mange sykehus, men dessverre ennå ikke ved vår avdeling p.g.a. manglende legekapasitet. Diagnosetolkningen krever spasialkunnskap hos patologen.
Punksjonscytologi / Finnåls aspirasjonsbiopsi
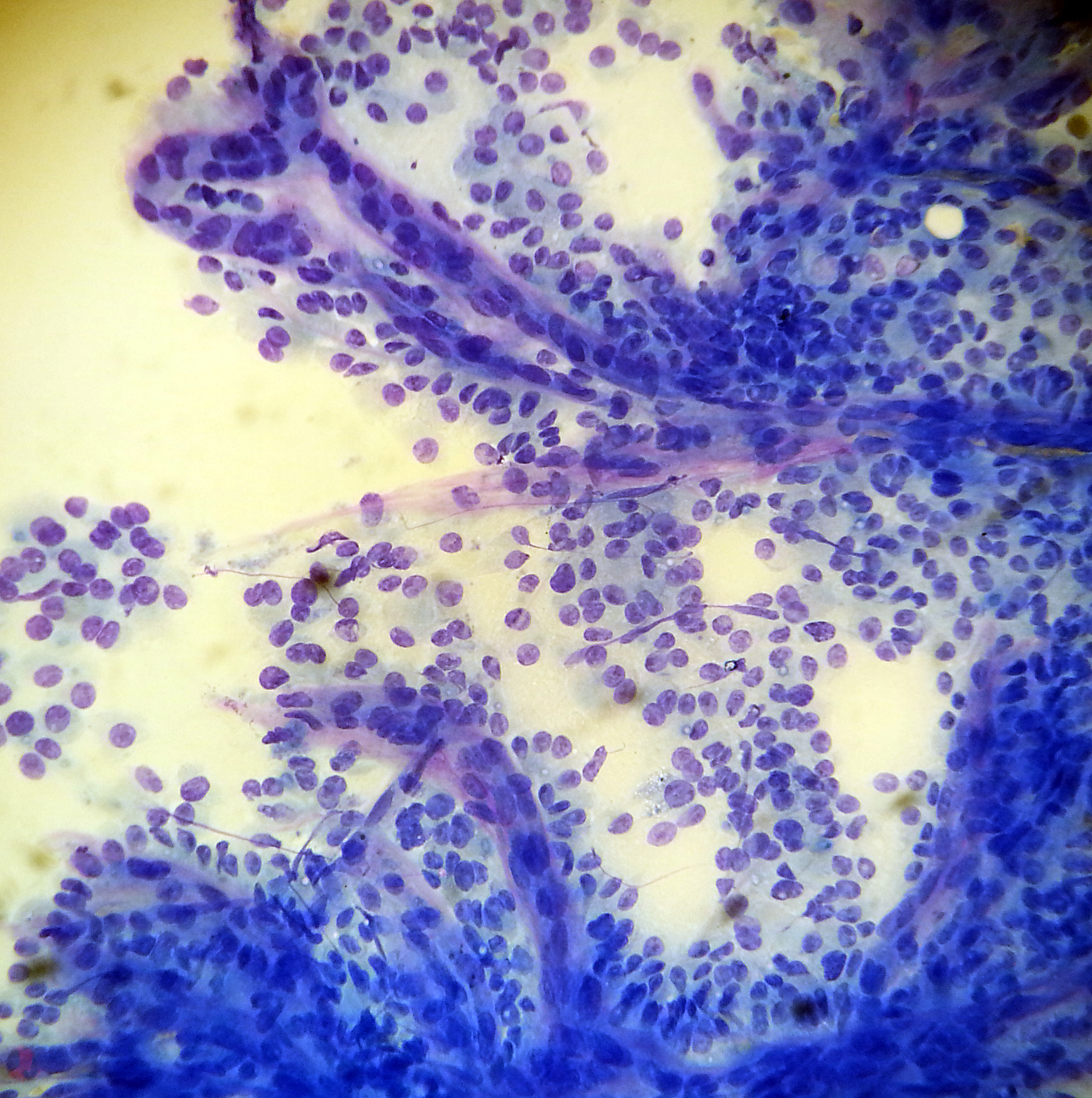 Dette er en hurtig og meget billig teknikk for at patologen
kan stille pasientdiagnoser. Særlig gjelder dette kreftproblematikk.
Dette er en hurtig og meget billig teknikk for at patologen
kan stille pasientdiagnoser. Særlig gjelder dette kreftproblematikk.
Patologen henter celler og små vevsbiter fra sykelige forandringer i kroppen hos pasienten ved hjelp av tynn nål og sprøyte. Patologen kan oftest i løpet av 5 til 10 minutter vurdere om det foreligger malignitet ( "kreft") eller ikke.
Nålen ( 25, 23 eller 22 G (gauge)) stikkes inn i området i kroppen hvor det er sykelige forandringer. Ved hjelp av hurtige og lett hakkende bevegelser av sprøyten ( 10 eller 20 ml) sammen med sprøyteundertrykk passer man på at materialet kommer i sprøytespissen og ikke i sprøyten. Ofte brukes en spesiell sprøyteholder (f.eks. Cameco). Rett etter sprøytes innholdet i sprøytespissen på ett objektsglass, blir strøket ut og hurtig lufttørket eller fiksert i fikseringsvæske (alkohol). Deretter farves materialet med hurtigfarvning (Diff- Quick). Patologen kan eventuelt stikke flere ganger for å få ønsket materiale til diagnosevurdering. Noen ganger , særlig hvis organet er blodrikt eller vevet lett lettoppløselig, kan patologen få materialet bare ved hjelp av nålstikk uten sprøyte, med hakkende bevegelse i det syke området hos pasienten. Noen ganger foreligger det ufarlig hulromsstruktur (cyste) og sprøyten blir fylt med væske som kan undersøkes videre av patolog på en avdeling for patologi.
Man kan stikke nålen i dybden i kroppen hvor man ønsker, nærmest uten å tenke på vev og organer nålen først går i gjennom. Materiale kan således hentes fra alle steder i kroppen. Det er så og si ingen komplikasjoner med teknikken.
Ubehaget for pasienten er som å få en sprøyte.
Har pasienten kjente unormale og udiagnostiserte knutestrukturer egner metoden seg utmerket som førsteundersøkelse. For å nå området i kroppen med forandringer kan patologen samarbeide med røntgenolog med ultralydveiledet punksjon. Ofte utføres dette med tynn slange ( f.eks. 3-way stopcock) koblet mellom sprøytespissen som røntgenologen veileder til målet og sprøyten som patologen bruker til å lage undertrykk.
For at metoden skal ha betydning må naturligvis materialet være adekvat og representativt. Prosedyren må også være korrekt. Erfaring med metoden og celletolkning er viktig.
Metoden har vært kjent fra før 1930, men er dessverre for lite brukt i Norge. Sverige er her et foregangsland hvor bl. a. Sixten Franzén var en hovedaktør. Ved visse steder i USA brukes metoden også hyppig. Metoden ville egne seg utmerket også i uland.
Noen fordeler med metoden:
1. hurtig og rask diagnosevurdering av patolog med erfaring
2. høy sensitivitet og spesifisitet for malignitet
3. ufarlig
4. ingen/ lite plage for pasienten
5. trenger meget lite utstyr
6. kan brukes poliklinisk og på sykehus
7. reduserer antall sykehusopphold for å få stilt diagnoser ("flere ledige senger")
8. mulighet for preoperativ diagnose og informasjon til pasienten før planlagt operasjon
9. reduserer hyppigheten av eksplorativ laparotomi og thoracotomi
10. diagnose hos inoperable pasienter, før annen behandling
11. unngår arrdannelse (arr kan bl. a. kan resultere i tolkningsvanskeligheter ved senere mammografi og også uheldig utseende av brystet)
12. ferdigbehandling (f.eks. ved noen cyster )
13. lett å gjenta.
14. kontrollmetode
15. høy kost- effektivitet
Ulemper:
1. må ha rik cytologi/ patologierfaring
2. mindre informasjon enn ved vanlig histologisk undersøkelse
Det utføres nå oftest "pistolbiopsi" fra tumor hvor man får ut en tynn vevssylinder som blir behandlet som histologisk materiale.
Forandringene
i vevet er da ofte lettere vurderbart for patologene i forhold til celleforandringer
i cytologisk materiale og gir også tilleggsinformasjon.
(særlig ved tumorpatologi, men også ved annen patologisk tilstand).
En tumor kan være helt ufarlig, men kan gi varierende og vedvarende plager. Andre svulster kan være mer eller mindre farlig og kan medføre døden, etter kort eller lengere tid.
Patologen vurderer biopsi- og cytologimateriale ofte tatt fra en tumorprosess. Vedkommende som er en klinisk legespesialist må da også tenke på at bak hvert mottatt materiale er det et menneske og familie med sine bekymringer. Patologivurderingen er for å sette det riktige navnet på tumoren (diagnosen) som pasienten lider av, om den er ufarlig eller graden av farlighet, vurdere funnene og også prognosen. Deretter kan pasientens lege gi den riktige behandling slik at pasienten ikke bli over- eller underbehandlet.
Patologen har kontakt med pasientens lege, men stort sett ikke direkte kontakt med pasienten. Patologen får dog i hvert tilfelle opplyst noen fakta angående pasienten.
Tiden fra tumor blir oppdaget til svaret fra patologen er avgitt, altså tiden hvor den virkelige diagnosen ikke foreligger og er usikker, er en psykisk vanskelig og problematisk periode for pasienten og familien. Intet presist om tumoren kan bli sagt før svaret fra patologen foreligger.
Pasienten får høre patologens diagnoseresultat og vurdering via sin lege . Resultatet kan ha en meget stor betydning både psykisk og fysisk for pasienten og vedkommendes sosiale krets. Behandlende lege og pasienten diskuterer videre fremdrift når svaret foreligger fra patologen. Svaret representerer den "tredje person" i diskusjonen, selv om patologen er in absentia.
For resten av livet vil pasienten ofte være avhengig av hva som foreligger og således patologens resultat og vurderinger.
Dette svaret gir også graden av behandling som man mener er nødvendig. Det er derfor meget viktig hva patologen formidler til behandlende lege.
Hvert svar influerer på pasientens psykiske og fysiske
helse.
Obduksjon
Autopsy (= obduksjon) in English, writer Ed Uthman, M.D, (U.S.A.)
Her utfører patologen (legespesialist i faget patologi) en grundig undersøkelse av en avdød pasient. Kliniske opplysninger angående pasienten, pasientjournal, omstendighetene og evntuelt funn i forbindelse med døden, ytre kroppsfunn, makroskopiske organfunn, mikroskopiske funn og rasultat av andre undersøkelser blir samlet vurdert for å komme frem til konklusjonene. Disse sier noe om den umiddelbare dødsårsak, hvilke lidelser som har ligget bak og evnt. andre lidelser som pasienten har hatt. Avdøde blir behandlet med respekt. Åpningene inn til kroppshulene som lages i forbindelse med en obduksjon syes pent igjen.
Det foreligger lov og forskrifter angående sykehusobduksjon som blir fulgt.
Bare lege kan rekvirere klinisk obduksjon! Bare politiet kan rekvirere rettsmedisinsk obduksjon!
P.g.a. for få patologer og for stort arbeidspress utføres på en patologiavdeling nesten bare diagnostiske undersøkelse av materiale tatt fra levende pasienter. I Norge er obduksjonsvirksomheten sterkt nedprioritert og har minket betraktelig i de senere år. I 1993 ble bare 14% mot anbefalt 40% av de døde undersøkt. Dette er et paradoks i forhold til satsningen på kvalitetssikring. Obduksjoner gir en meget god kvalitetskontroll på helsevesenets medisinske diagnostikk og behandling. Reduksjonen av antall obduksjoner gjør at man i Norge i praksis ikke sikkert vet hva de fleste folk dør av og landet har således en uriktig dødsstatistikk. Med stor satsning på kvalitet er dette urovekkende. F. eks. har det vist seg i studier utført i flere land at fra flere % opp til ca. 60%? av de kliniske diagnosene er mer eller mindre betydningsfulle feildiagnoser. Stort sett blir det funnet betydningsfulle forskjeller mellom kliniske diagnoser og obduksjonsfunn i ca. 20%. Dette gjelder f.eks. ofte lunge- og hjerteinfarkt. Mange av kreftforekomstene blir ikke klinisk funnet eller registrert. Ved såkalte "klare kliniske tilfeller" finner patologen ofte ved obduksjon overraskende eller oversette funn. Ved lav obduksjonsfrekvens blir den læremessige siden ikke ivaretatt og pårørende får ikke den informasjon som de ønsker.
Rettsmedisinske obduksjoner er dessverre også redusert i antall.
Vekst
Patologifaget er i kontinuerlig utvikling og vekst.
F.eks.:
Nye vurderingskriterier
Prognosevurderinger
Immunhistokjemi
Flowcytometri
Billedanalyse
Molekylærpatologi
Elektronmikroskopi
Klinikerne og nye kliniske undersøkelses- og operasjonsmetoder krever en stadig mere omfattende, detaljert og spesifisert diagnostikk og mest mulig eksakt diagnose. Dette for å kunne velge den beste behandlingsmetode og også bedre vurdere sykdomsprognosen. Det er nødvendig med stor og nøyaktig arbeidsinnsats fra alle ansatte ved en patologiavdeling og arbeidet krever godt utdannede medarbeidere for at patologen til sist skal komme til det endelige diagnoseresultat.
Avd. for Pat., SiV: Eneste sted i Vestfold fylke med patologiservice. Opprettet i 1980 med mål å dekke hele patologibehovet for Vestfolds fylke. Fine lokaler fra 1993 i øverste etasje i laboratoriebygget. Moderne og godt teknisk utstyrt. Leger- patologer og LIS-leger (ass.,leger), bioingeniører, kontorpersonale, obduksjonspreparanter). Forskning.
I Norge: Ca. 22 steder med patologivirksomhet,
hvorav to private. Antall biopsivurderinger utført fra vevsmateriale
som er tatt fra pasienter er økende, antall vurderinger fra cytologimateriale
er relativt uendret og antall obduksjoner er blitt færre.
Det foreligger mangel på patologer.
Kreft Cancer Svulst
Kreft (Cancer) er et gammelt navn som er gitt etter det makroskopiske bildet som ofte sees ved brystkreft, i det bildet kan ligne på en kjempekrabbe.
I dag er Cancer en generell betegnelse for ondartet tumor i kroppen. Det foreligger ukontrolert nydannelse av celler eller vev, som nærmest vokser på egen hånd.
Karcinom= ondartet epitelial tumor.
( Den mest vanlige tumorgruppe)
Utgår fra epitelvev som har en eller fler- laget/ radet epitel og som dekker ytre og indre kroppsoverflate.
Sarcom= ondartet mesenchymal tumor
( Relativt sjeldent)
Utgår fra mesenchymalt vev.
Mesechym er embryonalt bindevev eller ikke-epitelialt vev. Multipotent "morsvev" for alle former for støttevev og bindevev, tverrstripet muskelatur, nærmest all glatt muskulatur, hjertemuskulatur, karendotel (celler på indre karoverflate), blodceller og spesialiserte bindevevsceller.
Svulst
Hevelse av vev p.g.a. en eller annen prosess som f. eks. ødem ("væskeansamling i vev") betennelse, cellevekst og "stofflagring".
Til alle tider har det forekommet kreft. Slike forandringer er funnet hos mennesker som levde for 2000 år siden i Egypt og i India. Det er også sett i 5000 år gamle Inka-mumier. Dyr og planter kan også få kreft. Generelt har hyppigheten økt i de siste 100 år (Kreftstatistikk, men mye usikkerhet). Hvor hyppig kreft var tidligere vet man ikke. Hyppigheten er varierende i de forskjellige land og gjennom tid og for de forskjellige svulsttyper.
De fleste typer kreft synes å bli hyppigere. Noen krefttyper synes å minke i antall.
Årsak til kreftøkning?
1.Tilsynelatende økning på grunn av bedre/ annen diagnostikk/ svulstkriterier, både av klinisk lege (også pasient) og patolog.
2 Høyere levealder. Flere personer er således i den «kreftfarlige alder». (Barn/ yngre får relativt sjeldent kreft og da ofte spesielle krefttyper).
3. Tiltagende kreftmedvirkende årsaker og bruk/ forurensning av mulig kreftfremkallende stoffer (eks. røyk, alkohol).
Det synes å være mange faktorer til at kreft oppstår. Kreftfremkallende stoffer trenger lang innvirkning mot kroppen og en hvis mengde/ påvirkning for å kunne medvirke til at kreft oppstår. Blir mennesket påvirket av flere kreftfremkallende stoffer, mer eller mindre samtidig, kan ofte kreft lettere oppstå (F.eks. røking og asbestpåvirkning = mange ganger større sjanse for å få kreft enn ved bare asbestpåvirkning). Kreft har stort sett lang latenstid. Hormonelle omstendigheter og immunforsvar spiller også inn.
PHILOSOPHIA
De laanske sannheter! Skrevet tirsdag, 19. januar 1999
1. Noe er, og tankene registrerer dette.
2 Tiden består av/ kan bare registreres i form av strukturforandringer .
3. Strukturer er rom/ geografi.
4. Delene i strukturforandringene kan relativt bare fjerne seg eller nærme seg.
5. Det fins små- og stor- sykliske svingninger.
6. Kaoset er også organisert og intet er helt tilfeldig.
7. Alt innvirker mer eller mindre på hverandre.
8. Det eksisterer også ikke- struktur.
9. Alt har sitt rekkefølge.
10. Tiden står ikke stille, men tidsretningen er ukjent og kan ikke bedømmes.
11. Tidsoppfatningen er psykologisk betinget.
12. Hva som skjer kan ikke avgjøres i nuet.
Etikk må sees i forhold til kultur, sted og tid.
Alt kan ikke uttrykkes i ord.
Ingen har den samme oppfatning.
Det går ikke an å være alene.
Det som er, er ikke det normale og intet er normalt, men alt relativt.
Det fins bare relativt rettferdighet og intet er egentlig rettferdig.
Samfunnet er ikke klokt.
Alt er ikke mulig og alt kan ikke skje.

Alt innhold på Https://www.patologi.com eller no er beregnet til internt bruk av/ for eier © Har ikke ansvar for opphav, innhold o.l. fra eksterne nettsider/ lenker eller sider/ innhold på https://www.patologi.com eller no. Bruk utenom av andre personer gjøres på eget ansvar. Vær Varsom- plakatens regler for god presseskikk følges mulig ikke.
Norway. This WEB page was first created 19. May 1996.


Tønsberg 22.11.2016